免校准光镊,重磅Nature Physics,揭秘膜力学传播机制研究!
发布日期:2025-12-11
机械信息通过细胞骨架、细胞器和质膜进行传递,对细胞的组织结构与机械传导过程至关重要,并深刻影响细胞形态、信号传导及代谢活动。先前研究报道,质膜的膜库(membrane reservoir)特性及脂质双分子层的流体特性会导致膜张力在超过松弛时间后趋于恒定,局部外力引发的张力增加会迅速传递至整个膜表面。但近年研究发现膜张力传播存在显著细胞类型特异性,组织培养细胞中传播不明显,而神经元轴突中传播距离可达数十微米。为破解这一科学谜题,巴塞罗那科学技术学院的西班牙光子科学研究所团队借助西班牙Impetux的免校准生物型光镊-SENSOCELL展开专项研究,该系统凭借免校准即插即用、无需繁琐标定,飞牛级超高精度、多光阱同步操控、活细胞与组织原位测量及自动化软件支持的核心优势,为实验提供了高效精准的技术支撑,最终在秀丽隐杆线虫触觉受体神经元(TRNs)模型中取得突破性进展。

免校准生物型光镊-SENSOCELL
研究团队基于SENSOCELL开发了一种基于光镊的膜纳米流变学技术(membrane nanorheology),以秀丽隐杆线虫的触觉受体神经元(TRNs)作为轴突膜张力传递的生物物理模型,系统探究了轴突膜张力的传播调控机制及细胞外力响应适应机制。
研究人员设计了一组实验,利用单个分时激光源同时拉出两个膜系链(membrane tethers)。首先将单个激光源以25 kHz的频率进行分束,产生两个可以在二维独立移动的光阱(图1a,紫色和绿色)。然后,主动拉动光阱1(紫色)中的膜系链,并测量由光阱2(绿色)保持的静态膜系链的力学响应(图1b),可以明显看到,随着光阱1的主动移动,产生明显的膜张力,并且传递到光阱2。进一步研究发现触觉受体神经元(TRN)和DVA神经元的结果对比,发现膜张力在TRN中传播得更远、更快,说明表明膜张力传播的范围和速度具有细胞类型特异性。
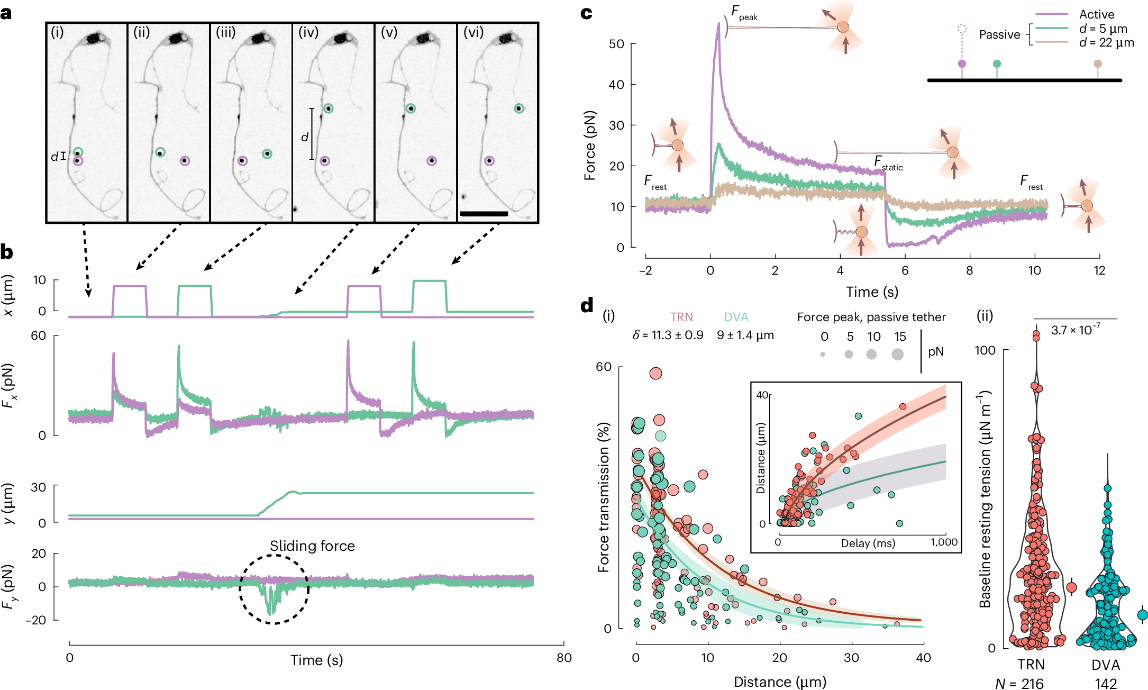
图1 用于测量膜张力传播的双光阱检测法
研究人员基于已有的膜张力传播模型开展计算机模拟,结果表明,张力传播过程显著依赖于膜的面内弹性、粘度及膜的渗透系数k。模拟进一步揭示,周期性排布的障碍物会降低膜的渗透率,从而限制张力沿轴突膜的传播范围(图2)。
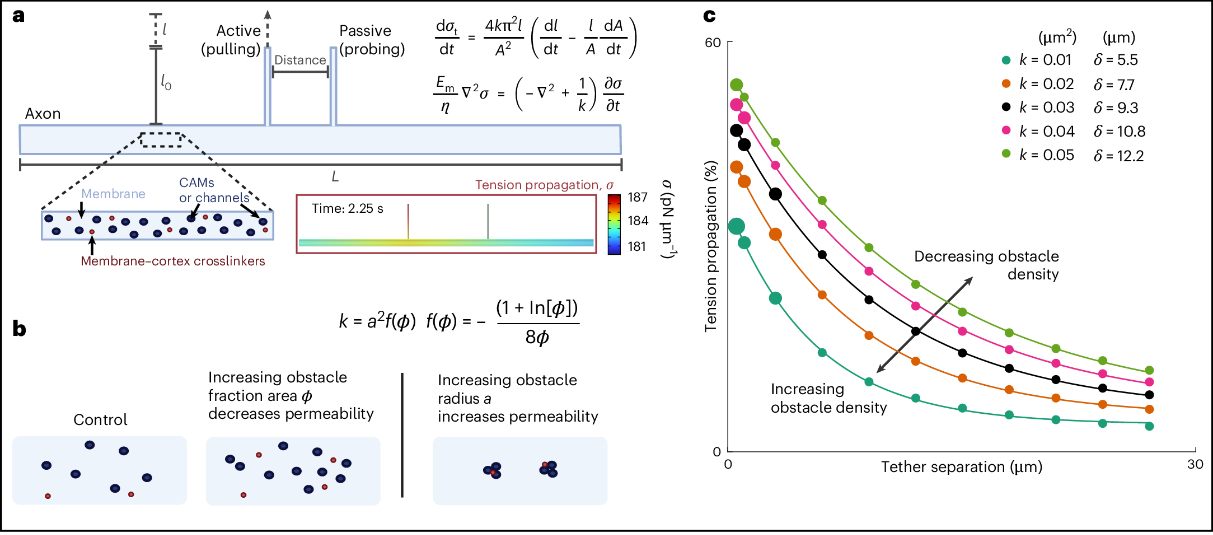
图2 膜张力传播的理论模型
先前的研究指出,与肌动蛋白细胞骨架相连的跨膜蛋白会阻碍膜中脂质的流动。基于这一认识,研究团队将膜与其下方的细胞骨架视作一种复合材料,并假设细胞骨架的改变会影响膜的渗透性。不同的处理条件下的张力传播和静态张力结果表明,神经元对肌动蛋白破坏的反应依赖于药物种类和浓度,且与LatA(能够隔离肌动蛋白单体,干扰肌动蛋白聚合)的急性处理相比,对CytoD(能够解聚动态肌动蛋白丝)更为敏感(图3a,b)。接着,研究组检测了微管是否调节沿膜的张力传播。与对照组相比,mec-12突变体(缺乏乙酰化的15-pf微管)表现出张力传播减少,并且Nocodazole诺考达唑处理导致了更多的减少(图3e,f),表明微管支持轴突中的膜张力传播。
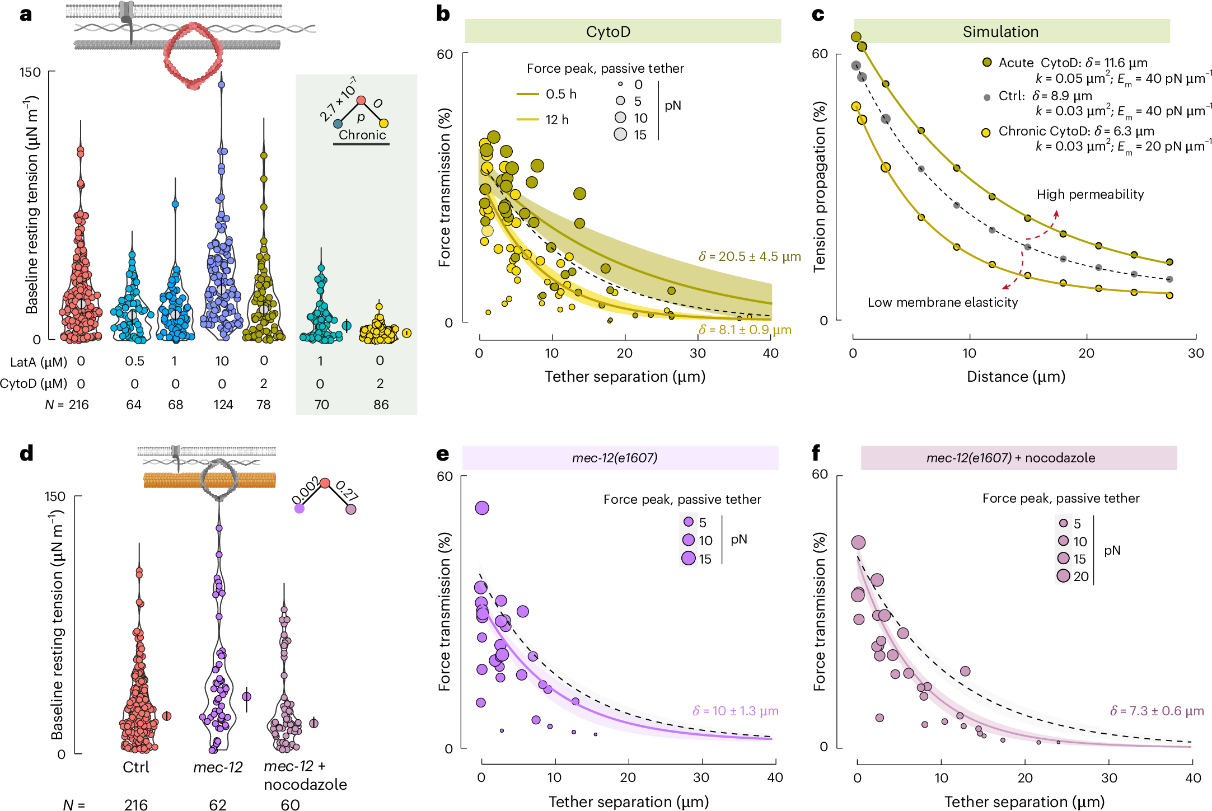
图3 F-肌动蛋白和微管网络的完整性影响张力传播
研究团队采用计算机模拟方法对血影蛋白细胞骨架进行建模,比较了随机分布与周期性排列的障碍物所产生的影响(图4b)。模拟结果表明,周期性的细胞骨架排列在短距离内能够增强张力传播。与模型预测一致(图4b),血影蛋白突变体在短距离内的张力传播程度低于野生型;而在unc-70缺失突变体的神经突中,张力可传播至显著更远的距离(图4c)。综合实验与模拟结果可知,周期性的膜障碍物及其相关细胞骨架成分能够在局部限制并界定膜张力传播的范围。
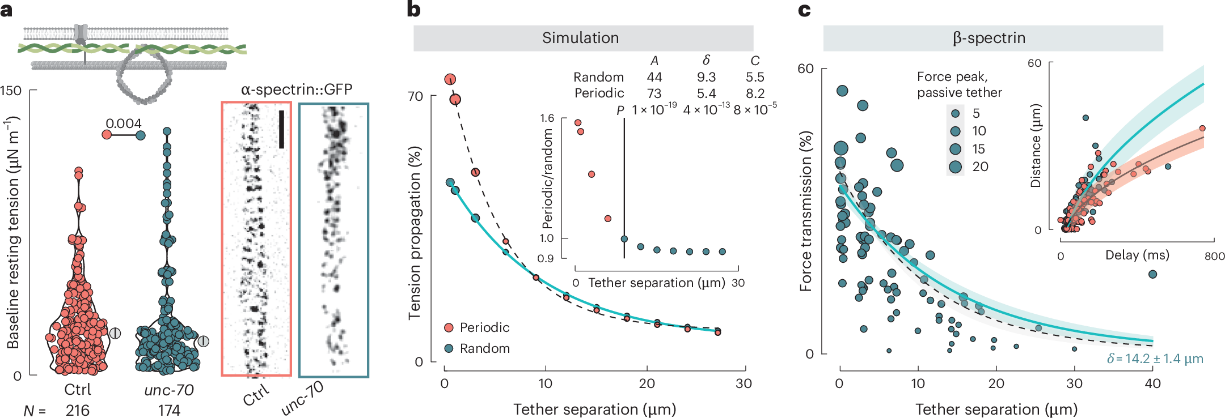
图4血影蛋白细胞骨架的周期性有助于短距离内的张力传播
最后,研究人员验证了膜上的障碍物是否确实会影响膜张力的传播。Stomatin同源蛋白MEC-2会在质膜上形成凝聚体,且能够结合胆固醇,使膜变得更硬。在MEC-2基因敲除动物中进行的连接拉伸实验发现,静息膜的基线张力低于对照组神经突(图5a),张力传播显著增加(图5b);使用甲基-β-环糊精(mbCD)处理细胞以去除膜胆固醇也能增加张力传播(图5d)。这些数据表明 MEC-2 凝聚体作为一种障碍物,通过与膜中的胆固醇相互作用来限制膜张力的传播。
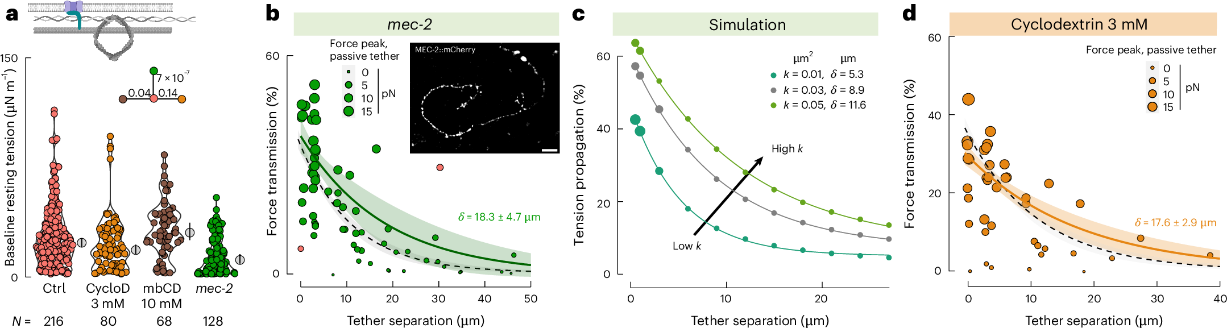
图5 MEC-2在膜上的凝聚限制张力传播
研究团队以秀丽隐杆线虫为模型,探究了机械应力沿感觉神经突膜传播的分子机制。基于SENSOCELL光镊系统的膜系链拉伸实验结果显示,膜张力的传播行为与生物物理模型的预测相符:膜-皮层结构的破坏导致膜通透性升高(障碍物密度降低),从而使张力传播距离增加;周期性的障碍物排列支持短距离内的张力传播,而更均匀、随机分布的障碍物则有利于张力进行长距离传播。
在此项研究中,研究团队采用的免校准生物光镊系统SENSOCELL能够在无需复杂校准的前提下,实现对捕获微球的高精度空间操控与力学测量。SENSOCELL可控制微球沿预定轨迹逼近细胞表面或从膜上脱离,同时实时、高精度地同步记录施加于微球的力与位移信息。通过对力‑位移曲线的分析,可直接推演出细胞膜中的张力分布。此外,该系统支持多光阱并行操作,可在同一细胞表面同步操控多个微球、构建多条膜连接,从而实现在空间上解析机械力沿细胞膜的传播特性。
SENSOCELL 光镊系统核心优势:
免校准即插即用:无需繁琐标定流程,开机即可开展测力实验,新手也能快速上手,大幅降低科研准入门槛;
飞牛级超高精度:力学分辨率高达 50fN,定位精度<1nm,可精准捕捉细胞微小力学变化,为实验数据提供可靠保障;
多光阱同步操控:支持高达 256 个光阱同步操作,可自定义轨迹、振荡、拖拽等动作,实验自由度极高,满足复杂实验设计需求;
原位测量能力突出:不仅适用于细胞、细胞核、囊泡等内源结构,还能深入组织内部开展力学检测,真正实现活细胞与组织的原位测量;
自动化软件赋能:LightAce 软件基于 ImageJ、μ-Manager 开发,界面友好且支持自定义实验流程,可显著提升科研效率。
参考文献:
[1]. Català-Castro, F., Bonilla-Quintana, M., Sanfeliu-Cerdán, N., Rangamani, P., & Krieg, M. (2025). Obstacles regulate membrane tension propagation to enable localized mechanotransduction. Nature Physics, 1-12.


