无固定无标记原生成像!实验室台式软X射线细胞结构显微镜技术革新与神经退行性疾病研究进展
发布日期:2026-05-12
引言
软X射线断层成像(Soft X-ray Tomography, SXT)历经三十余年发展,已从概念验证性的显微成像技术,演进为高通量定量成像模态,可直接解析完整细胞的亚细胞结构、定量细胞器化学成分变化,并构建数字细胞模型以揭示细胞动态行为,为细胞生物学核心科学问题提供全新解决方案。
SXT的核心成像原理基于软X射线在“水窗”区域(能量范围284–543 eV,波长4.4–2.3 nm)内生物材料的本征吸收特性。在此能量范围内,X射线与物质的相互作用主要通过光电吸收实现,散射等其他过程可忽略不计,因此线性吸收系数(Linear Absorption Coefficient, LAC)与参与X射线相互作用的原子数量成正比,可精准反映氨基酸、碳水化合物、脂质等分子的组成与浓度。不同细胞器具有特征性的LAC值,例如细胞核LAC约为0.26 μm⁻¹,线粒体LAC约为0.32–0.36 μm⁻¹,脂滴LAC高达0.48–0.90 μm⁻¹。这种结构 + 成分双维度定量能力,是传统光学显微镜与电子显微镜难以实现的。
伴随实验室台式 SXT 技术的成熟,SiriusXT公司研发的商业化实验室型软X射线显微镜SXT-100,突破同步辐射大装置的使用限制,可在常规实验室环境下对完整冷冻含水细胞与组织切片实现纳米级三维无损成像,为神经退行性疾病的致病机制解析与靶向药物开发提供了可及性更高、应用更灵活的前沿成像平台。
1. 实验室级SXT的技术革命:SXT-100核心能力分析

Weinhardt与Larabell(2025)在《Annual Review of Analytical Chemistry》综述中系统界定了 SXT 相较于传统成像技术的核心优势。SXT-100将同步辐射级成像能力集成于紧凑型实验室桌面平台,占地面积仅为2 m × 3 m,单次完整断层扫描仅需85分钟,实现了同步辐射级成像能力的实验室级替代,大幅降低技术使用门槛。

基于该综述所确立的技术评估体系,SXT-100的核心能力可归纳为以下四点:
(1)无需固定、无需标记的原生态成像
SXT的价值在于能够在不使用固定或染色的情况下对完整细胞进行三维成像,同时提供丰富的化学成分信息。综述强调,SXT能够以近原生状态对完整冷冻保存的细胞进行三维成像,覆盖从细菌到真核哺乳动物和人细胞在内的多种细胞类型,穿透直径达20–25 μm的完整细胞,空间分辨率为25–60 nm。
SXT‑100 在此基础上进一步优化:
空间分辨率达40–50 nm;
可对 10–15 μm 厚组织切片直接三维断层扫描;
全程无需化学固定与物理切片,彻底规避传统制样导致的结构伪影;
适用于细菌、哺乳动物细胞、人源原代细胞等多种样本类型,保持细胞最接近生理状态的结构信息。
(2)基于线性吸收系数(LAC)的定量分子信息
不同细胞器具有特征性的LAC值范围:脂质是细胞内吸收能力最强的组分之一,LAC通常高于0.5 μm⁻¹,主要归因于其高碳浓度;叶绿体和线粒体均参与葡萄糖代谢和ATP合成,LAC值介于0.3–0.4 μm⁻¹之间;而细胞核在大多数细胞类型中的平均LAC值保持在约0.25 μm⁻¹的保守水平。这种差异吸收特性为细胞器的分割和结构分析提供了重要工具。
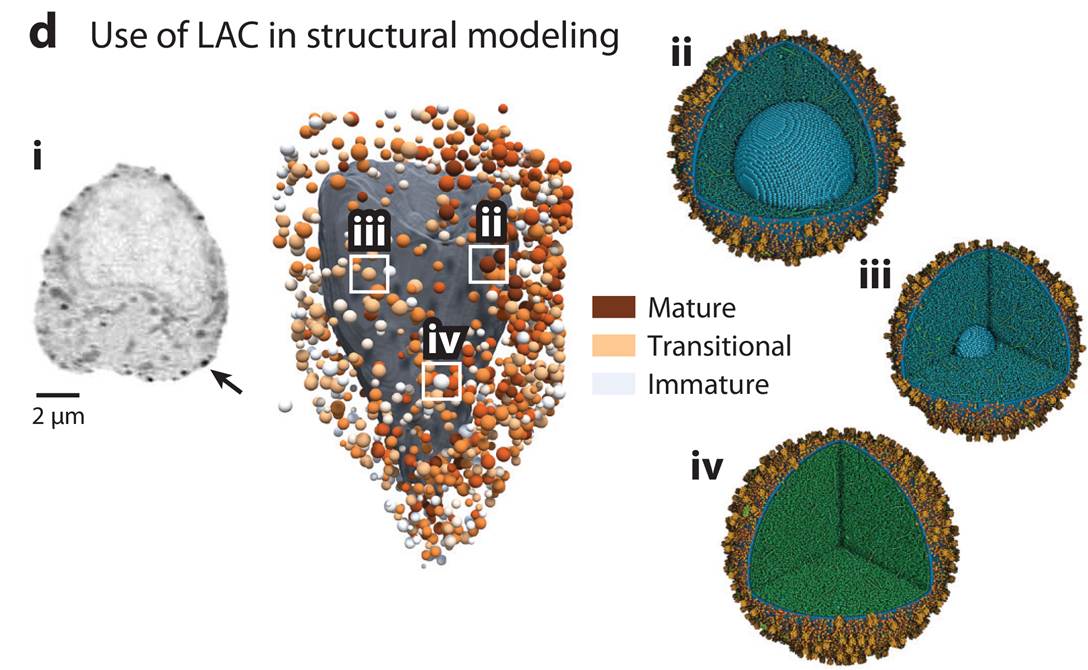
LAC的定量特性进一步推动了分子层面的数字建模突破。综述特别提及了David S. Goodsell团队的里程碑式工作——将SXT的LAC值与蛋白质组学、结构生物学和冷冻电镜数据相结合,成功在单体水平上对胰岛素颗粒在三个成熟阶段的组成进行了整体建模。这一工作充分展示了LAC值在细胞器分析中的强大潜力:例如,现已可能在不经标记的情况下确定实验操作后胰岛素颗粒的成熟阶段,甚至在患者组织样本中进行分析。展望未来,基于人工智能的蛋白质结构分析(如AlphaFold)与SXT所提供的定量信息的结合,将使得在分子水平上解读整个细胞成为可能。
(3)集成荧光的多模态关联成像
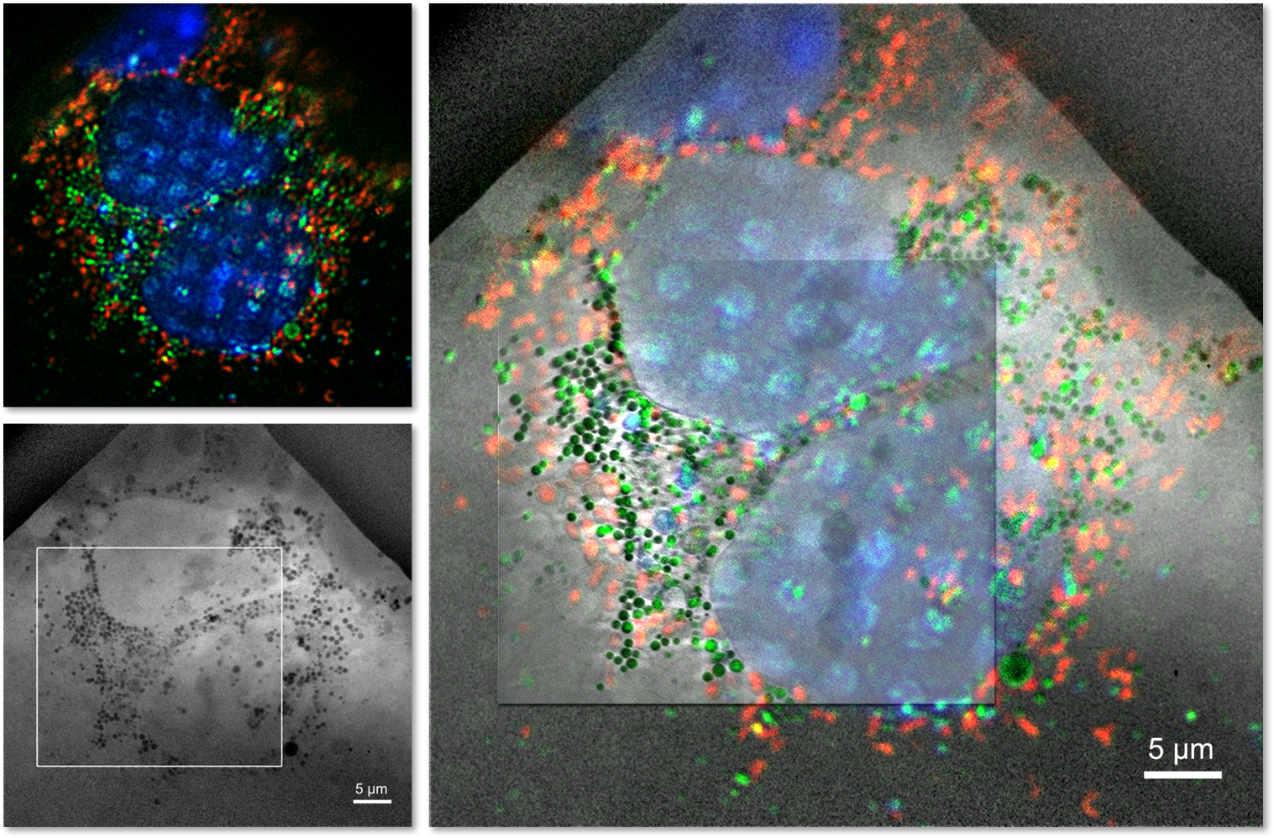
SXT-100在实验室平台中集成了荧光显微镜功能,实现了综述中所阐述的“冷冻荧光显微镜确定标记分子位置→同一标本SXT成像生成高对比度三维重建”的关联工作流程。成像后的样本仍可进一步用于冷冻电镜(cryo-EM)或冷冻电子断层扫描(cryo-ET),形成“光-电-射线”多尺度关联成像工作流(CLEXM)。综述指出,实验室系统往往具有更强的多功能性——由于X射线的日常可用性不受限制,能够在样品制备策略创新、新图像采集策略开发、更高生物安全级别设施中的成像以及SXT成像新应用领域的探索等方面取得进展。
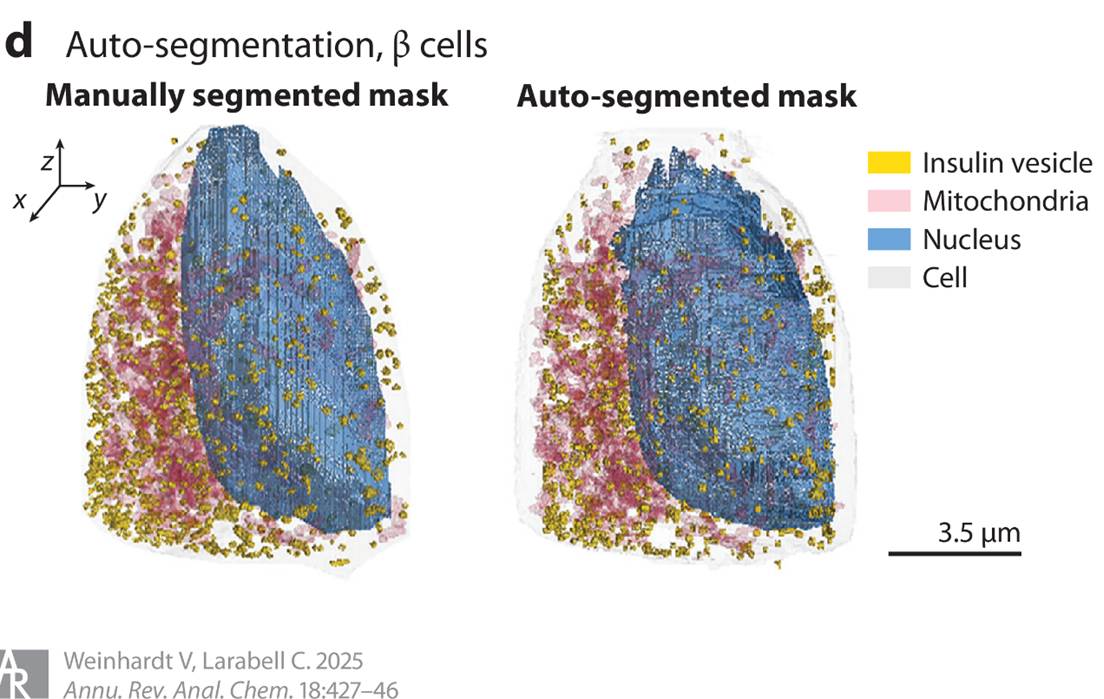
(4)自动化数据分割与深度学习分析
随着SXT系统通量的不断提高,对加速图像分析的需求也日益增长。综述指出,SXT图像与传统光学显微镜和电子显微镜图像存在本质区别——由于不使用重金属染色或荧光探针,细胞器之间的差异对比更为微妙,更接近于原生状态。因此,为电镜数据开发的基于对比度差异的分割算法无法直接应用于SXT数据。为此,SXT领域已开发出多款专用的半自动和全自动分割工具,以及多种基于深度学习(如卷积神经网络CNN)的分割模型。
综述进一步指出,一些CNN模型已被推广用于自动分割不同细胞类型。例如,针对酵母细胞开发了基于荧光标记训练的CNN模型,能够对液泡融合状态进行分类,并可分析液滴大小和脂噬现象——后者是一种重要的细胞通路,与退化性疾病中错误折叠蛋白的清除密切相关。
除自动分割外,综述还重点介绍了数据驱动的细胞建模前沿进展。David S. Goodsell团队将SXT的LAC值与蛋白质组学、结构生物学和冷冻电镜信息相结合,成功在单体水平上对胰岛素颗粒在三个成熟阶段的组成进行数字建模。这一突破性工作表明,结合AlphaFold等人工智能驱动的蛋白质结构分析工具,SXT的定量信息有望在未来实现对整个细胞在分子水平上的解读。这一技术路线对于理解神经退行性疾病中蛋白质构象异常与亚细胞结构重塑之间的因果关系,具有深远的应用前景。
2. SXT在生物医学研究中的应用全景
综述对基于SXT成像的出版物进行了系统的统计分析,揭示了SXT的核心应用方向:
细胞表型与细胞器结构重塑分析;
纳米颗粒‑细胞相互作用与胞内转运追踪;
病毒感染诱导的亚细胞结构动态变化研究。
SXT已被应用于涵盖细菌、酵母、藻类、原生动物、病毒以及原代细胞和永生化细胞系在内的几乎所有主要生物样本类型,充分体现了其作为“生物研究多用途工具”的广泛适用性。
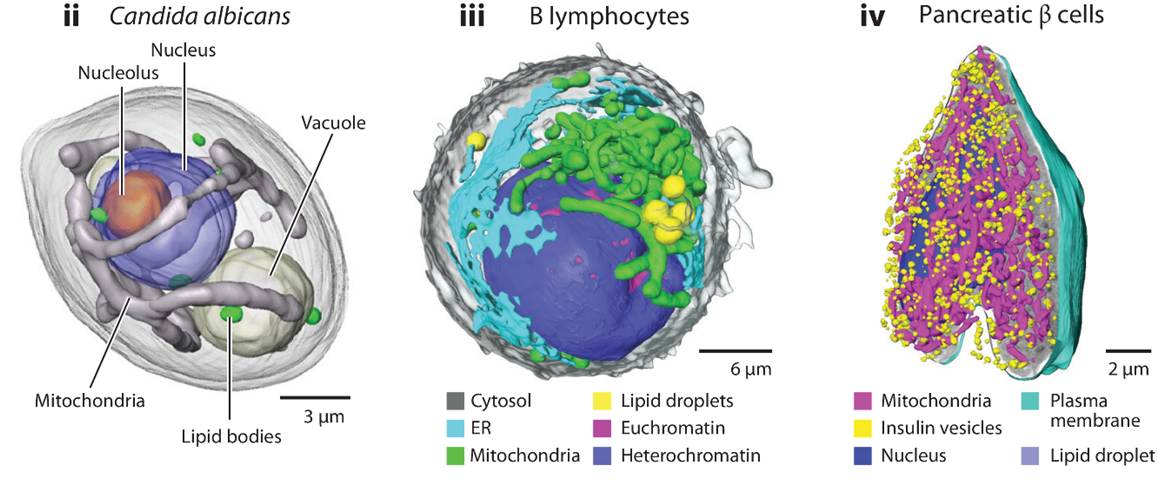
在疾病机制研究方面,综述特别指出,SXT的灵敏度使其能够在无需化学固定或染色的条件下,获取任何细胞中细胞器和特征结构的三维信息。该技术已被广泛应用于分析四种酵母物种在环境条件变化或突变情况下的结构改变,以及大量永生化细胞系在暴露于外部化学物质或物体(如纳米颗粒和病原体)时的结构响应。自新冠疫情以来,SXT在病毒研究中关于感染过程中细胞重塑的应用显著增加。
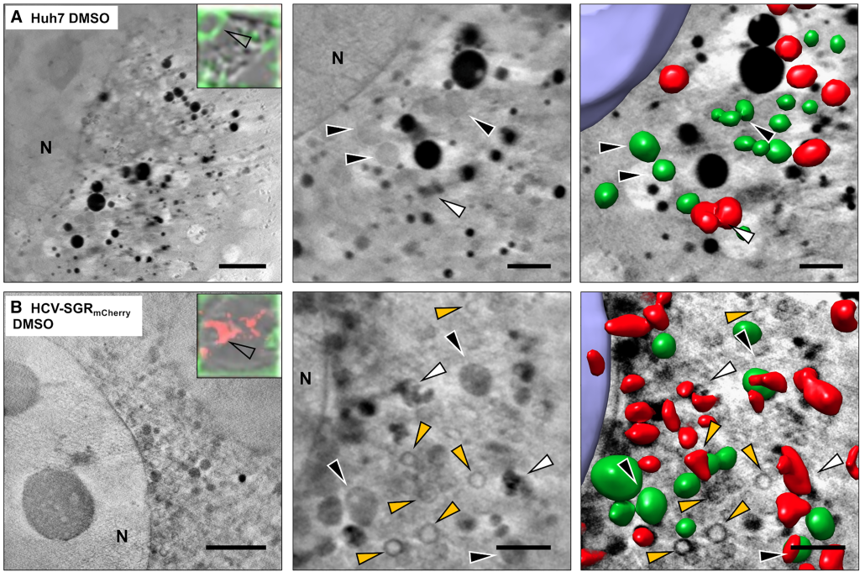
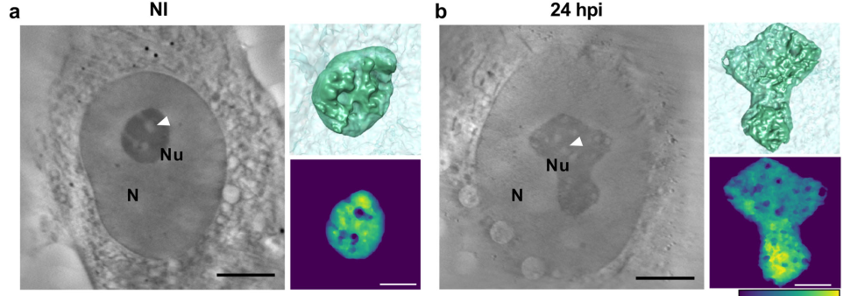
在知识产出方面,综述以犬细小病毒(CPV)感染为实例进行了详细说明:研究发现衣壳蛋白VP2的核仁定位信号能够与核仁蛋白相互作用,导致纤维中心/致密纤维组分界面的重建,促使核仁磷蛋白和上游结合因子等关键蛋白发生显著重组。该研究充分展示了SXT在捕获病毒诱导的亚细胞结构重塑方面的高度灵敏性。此外,综述还提及MISTRAL线站将SXT与X射线荧光元素分析相结合,成功用于理解纳米颗粒与细胞的相互作用。
3. 专题聚焦:SXT-100在神经退行性疾病研究中的应用路径
依托综述确立的技术体系与应用范式,SXT‑100 为神经退行性疾病机制研究与药物开发提供三条明确、可落地的技术路径:
(1)无膜细胞器相分离异常的定量可视化
无膜细胞器(如核仁、应激颗粒、Cajal体等)通过液-液相分离调控转录、剪接和RNA代谢,其相变失调与肌萎缩侧索硬化症、额颞叶痴呆等多种神经退行性疾病密切相关。综述明确指出,在研究膜性细胞器(如线粒体、内质网)和非膜性结构(如核仁、核斑、Cajal体)时,SXT的定量能力发挥着重要作用。这些结构和细胞器在细胞中具有高度动态的特性,其结构变化与多种生理和病理过程密切相关——例如线粒体的形态变化可能与细胞代谢、能量供应及疾病发生相关,而核仁的结构变化可能影响RNA的合成和加工。

SXT‑100 核心价值:
SXT-100对化学成分的高灵敏度和LAC定量能力,可无标记区分相分离形成的无膜区室;
定量监测核仁结构重塑、应激颗粒组装 / 解聚的动态过程;
以统计学水平评估致病突变对相分离行为的影响,提供分子组成与结构变化的定量证据。
(2)致病蛋白聚集体的亚细胞定位与原位结构分析
阿尔茨海默病中的tau蛋白神经原纤维缠结、帕金森病中的α-synuclein路易小体形成等蛋白聚集事件,其亚细胞定位和原位结构信息对理解毒性机制至关重要。SXT-100的集成荧光-SXT关联成像功能,可在三维结构图像上精准定位荧光标记的特定致病蛋白聚集体。结合综述中描述的LAC定量能力——即LAC的变化可作为细胞器组成变化的定量度量——研究者可以进一步分析聚集体周围亚细胞环境的分子密度和组织状态异常,为理解蛋白聚集如何引发局部细胞器功能障碍提供直接结构证据。
(3)纳米药物载体的靶向递送与内吞转运追踪
综述强调,纳米颗粒–细胞相互作用是SXT应用的重要方向之一。SXT-100已被成功验证可用于追踪细胞中荧光聚苯乙烯纳米颗粒的溶酶体共定位,并提供荧光信息与纳米药物递送载体在细胞内的三维共定位数据。此外,综述中指出MISTRAL线站将SXT与X射线荧光元素分析结合,已被成功用于理解纳米颗粒与细胞的相互作用。将上述方法扩展至神经元细胞模型,可在近原生状态下直观揭示神经保护药物载体跨越血脑屏障、被靶细胞摄取并与内吞-溶酶体系统相互作用的全过程,为优化靶向递送策略提供关键的三维结构依据。实验室系统的日常可用性优势使得在多次给药条件下对药物载体进行时间序列追踪成为可能,可定量评估纳米载体在神经元细胞内的靶向效率和亚细胞分布动态。

4. 总结与展望
SXT能够在不使用固定或标记的情况下可视化细胞,实现对细胞器化学组成和三维结构的定量分析。SXT-100作为创新性商业化实验室型软X射线细胞结构显微镜,具有紧凑小型化、快速成像、多模态关联、自动化分析、无机时限制等突出优势,在成像策略创新、高等级生物安全成像、新型样本制备与长期动态观测等方面具备难以替代的灵活性。
对于那些致力于破解神经退行性疾病中亚细胞致病机制、开发下一代靶向纳米治疗策略的研究团队而言,SXT-100以近原生态、纳米分辨率、定量 LAC、多模态联动的完整能力,为无膜细胞器相分离、致病蛋白聚集、纳米药物胞内转运等核心科学问题提供全新解决方案,是连接基础结构细胞生物学与转化医学的前沿工具。随着自动化细胞解剖技术的持续成熟,SXT‑100 将在神经退行性疾病机制解析、药物筛选与疗效评价中发挥更广泛、更深入的支撑作用。
参考文献
[1]. Weinhardt, V., & Larabell, C. (2025). Soft X-Ray Tomography Has Evolved into a Powerful Tool for Revealing Cell Structures. Annual Review of Analytical Chemistry, 18(1), 427–446.


