跨越尺度,触摸生命的“力量”:SENSOCELL免校准光镊助力细胞内力学进入定量时代
发布日期:2026-02-03
在生命科学的舞台上,细胞不仅演绎着精密的生化反应,更是一台时刻处于力学动态平衡的“微型机器”。从胚胎初始分裂时展现的刚性,到衰老过程中组织逐渐流露的柔软,这些微观的力学特性,实则是驱动发育、维持稳态、影响疾病进程的物理基石。然而,长久以来,科学家们缺少一种工具,能够直接、定量且无扰地深入活细胞内部,去测量一个细胞器的刚度,或解析一次分裂过程的力学驱动逻辑。
传统光镊技术虽能操控微粒,但其在复杂活体环境中的应用,常受限于侵入性损伤、繁琐的校准流程,以及对动态过程测量的乏力,西班牙Impetux公司开发的免校准生物型光镊系统 SENSOCELL,凭借其特有的 “直接光动量检测”技术,正在帮助全球实验室突破边界,将定量力学测量实验室“搬入”活细胞乃至活体生物内部。近期发表于《自然》系列期刊的两项里程碑研究,为我们揭示了这一平台如何解决领域内长期存在的核心难题。
挑战经典:无需完整收缩环,细胞如何分裂?
细胞通过收缩环一分为二,是教科书中的经典模型。但对于斑马鱼等胚胎细胞,其巨大的体积和卵黄使得完整的环无法形成。一个开放的、不闭合的肌动蛋白带,如何能产生足够且稳定的力来完成分裂?这成为发育生物学中一个悬而未决的物理谜题。
马普所Brugués课题组最近在Nature上发表的研究[1],颠覆了传统认知。作者发现,驱动分裂的关键并非一个静态的结构环,而是一个由细胞质自身刚度周期性变化所驱动的 “力学棘轮”。
研究揭示,在细胞分裂间期,遍布细胞质的微管星体网络使细胞质变硬,如同一个刚性的模具,为正在生长的肌动蛋白带提供稳固的锚定与支撑。此时,尽管带在生长,却难以向内深陷。进入分裂期(M期),微管解聚,细胞质显著流体化,肌动蛋白带得以快速向内收缩,推动分裂沟形成。然而,流体化也带来了不稳定,导致带体两端回缩。
那么,分裂最终如何完成?奥秘在于胚胎快速的细胞周期。当进入下一个间期,细胞质重新硬化,肌动蛋白带再度被稳定;随后的M期,内陷继续。这种 “硬化-稳定生长”与“软化-高效内陷” 的循环,在多个周期中如同棘轮般交替作用,最终在未形成完整环的情况下,逐步将细胞分开。这一精妙假说的定量验证,离不开对细胞质粘弹性的原位测量。研究人员利用SENSOCELL的主动微流变技术,直接在活胚胎内操控微粒,测量了间期与M期细胞质的复数剪切模量,发现间期的储能模量(G‘,弹性)与损耗模量(G’‘,粘性)在所有测量频率下均系统性高于M期。正是SENSOCELL提供的这份定量的、频率依赖的流变谱,为“力学棘轮”模型提供了坚实的物理证据,将定性的生物学观察转化为可计算的力学原理。
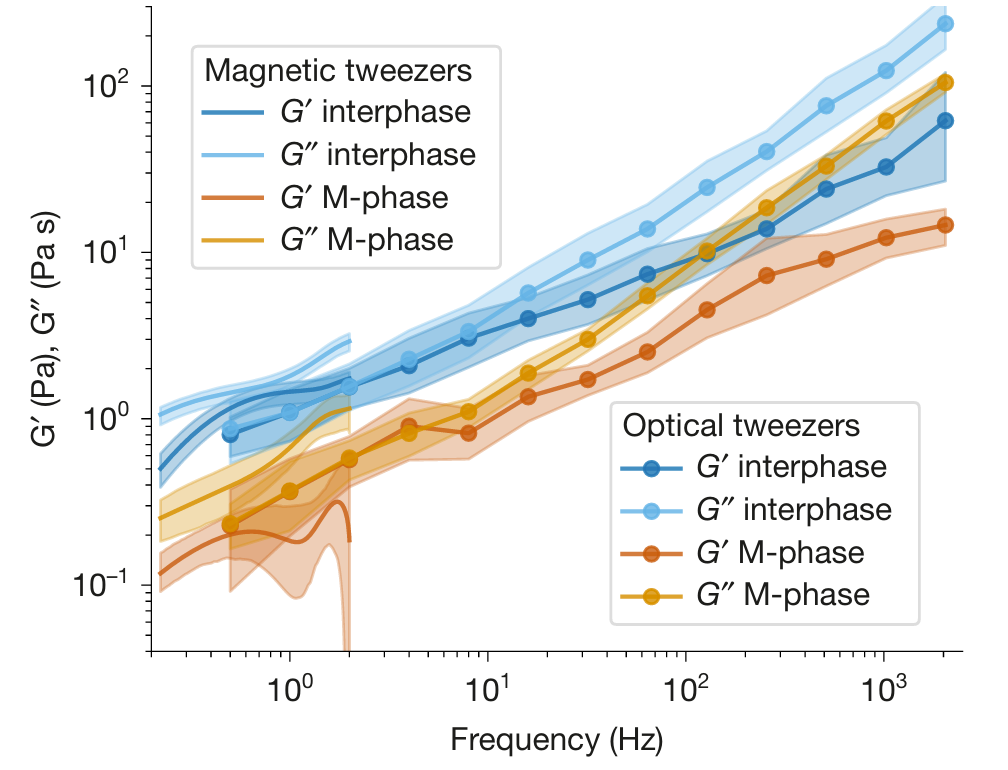
图一:定量分析比较细胞分裂间期和分裂期的储能模量G‘与弹与损耗模量G’’与频率关系
描绘衰老:从细胞器软化到生物体的“力学早衰”
上述研究解析了生命起始的力学法则,那么另一项发表于Nature Nanotechnology的工作[2],则利用同样的技术,绘制了生命衰老的力学图谱。研究团队利用SENSOCELL的主动微流变技术,实现了从亚细胞器到活体组织的跨尺度力学探测。在斑马鱼细胞内,作者成功测量了细胞质、核膜界面乃至细胞核核浆的粘弹性,首次在活体中揭示了细胞核不同区室间特异的力学分区,发现核膜刚度主要由核周肌动蛋白而非核纤层蛋白决定。
更具开创性的是,为了在活体模式生物秀丽隐杆线虫中进行长期无扰监测,团队创新性地将其肠道内丰富的内源性脂滴“改造”为天然力学探针。通过SENSOCELL操控这些脂滴,团队发现野生型线虫的肠道细胞质会随衰老显著“软化”。
研究人员分别在年轻(第1天)与年老(第8天)成虫的肠上皮细胞质中实施主动微流变测量。线虫细胞质刚度约为斑马鱼细胞质的十倍,阻碍了在胞内移动脂滴以使用同一探针检测多个区室。年老个体中这种类固体特征显著减弱,表明细胞质粘弹性在衰老过程中发生流体化转变。在导致核膜病与早衰表型的突变株中进行的主动微流变测试中,发现年轻成虫的lmn-1突变体细胞质粘度显著下降至年老野生型水平,且在最高龄样本中未进一步变化,表明lmn-1缺陷能够导致细胞质流变学特性发生早衰性改变。
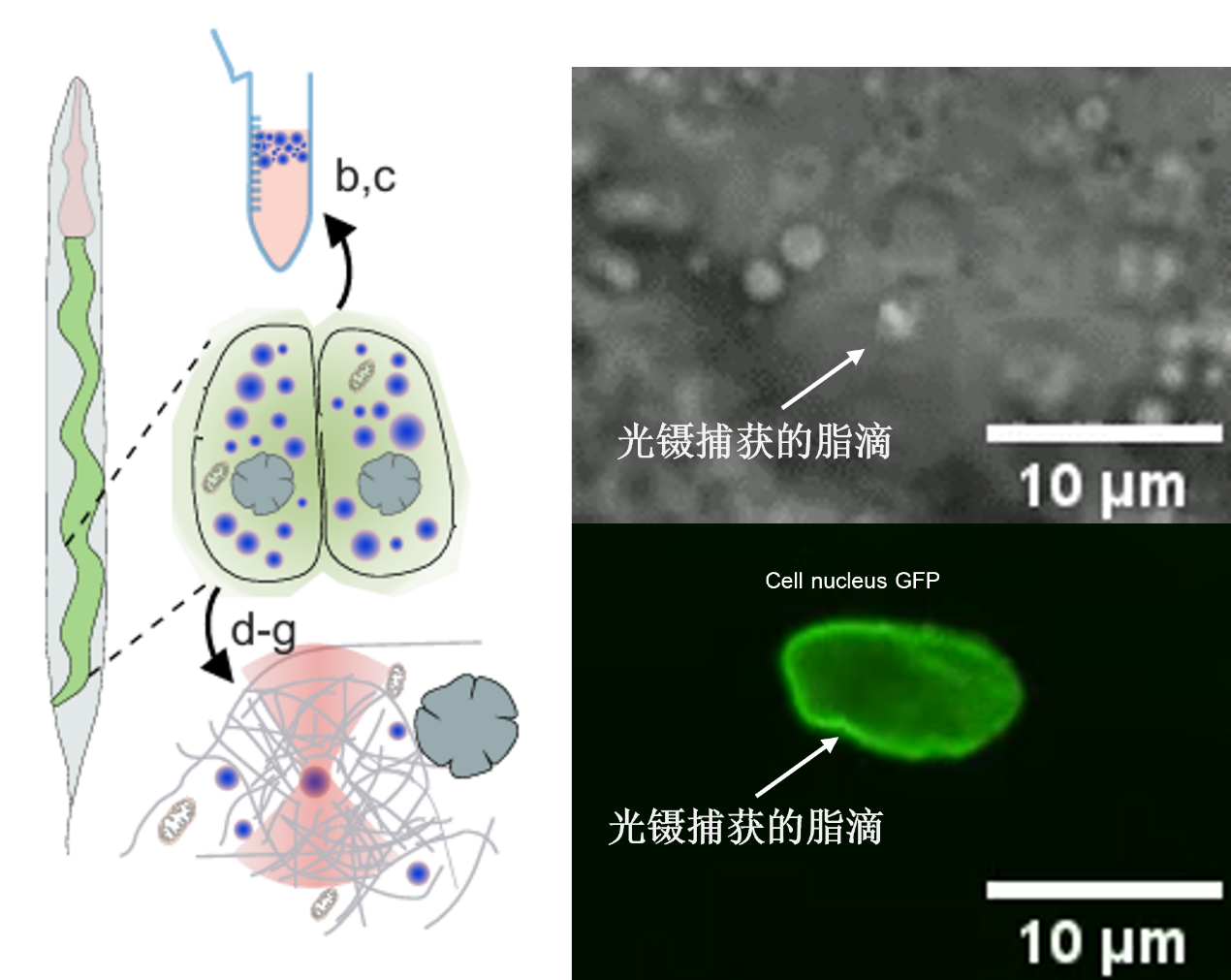
图二:光镊捕获脂滴进行微流变实验,研究核膜界面的粘弹性
这两项突破性工作都使用SENSOCELL的免校准光镊系统,通过免校准的直接测细胞内受力的特性,实现长期、动态的力学监测。同时此系统不像常规光镊必须以小球为抓手,而是生物自身结构作为探针,帮助研究者捕捉到了早于形态变化的“力学早衰”信号,为衰老及相关疾病提供了全新的生物物理标志物与研究方向。
SENSOCELL 光镊系统核心优势:
免校准即插即用:无需繁琐标定流程,开机即可开展测力实验,新手也能快速上手,大幅降低科研准入门槛;
飞牛级超高精度:力学分辨率高达 50fN,定位精度<1nm,可精准捕捉细胞微小力学变化,为实验数据提供可靠保障;
多光阱同步操控:支持高达 256 个光阱同步操作,可自定义轨迹、振荡、拖拽等动作,实验自由度极高,满足复杂实验设计需求;
原位测量能力突出:不仅适用于细胞、细胞核、囊泡等内源结构,还能深入组织内部开展力学检测,真正实现活细胞与组织的原位测量;
力学检测-成像一体化:系统支持宽场,共聚焦等不同成像技术,可以实现原位的力学检测-荧光成像;
自动化软件赋能:LightAce 软件基于 ImageJ、μ-Manager 开发,界面友好且支持自定义实验流程,可显著提升科研效率。

免校准生物型光镊系统 SENSOCELL
参考文献:
[1]. Kickuth, Alison, et al. "A mechanical ratchet drives unilateral cytokinesis." Nature (2026): 1-9.
[2]. Català-Castro, Frederic, et al. "Measuring age-dependent viscoelasticity of organelles, cells and organisms with time-shared optical tweezer microrheology." Nature Nanotechnology 20.3 (2025): 411-420.


