告别“抓不住、测不准”!单细胞显微操作系统,助国内团队接连登顶国际期刊
多功能单细胞显微操作系统- FluidFM OMNIUM是一款融合原子力显微镜与微流控技术的高端表征工具。其核心技术FluidFM采用纳米级中空探针,可实现单细胞/微球秒抓秒放,全程无损伤,为科研领域提供了精准的数据支撑。该技术配备300纳米孔径的微流控探针,可以稳定捕捉直径仅数百纳米到数微米的样本,有效避免测试过程中样本断裂或变形,成功解决传统设备 “抓不住、测不了” 的困境;同时通过方程拟合测试数据,能实现对样品弹性模量的定量分析,弥补了传统动态力学分析(DMA)等方法在超细样品测量中的局限性。近期,依托FluidFM技术,国内科研团队捷报频传,西湖大学与北京大学的相关研究成果分别发表于 Nature Communications 和 Journal of Controlled Release 等知名期刊,彰显了 FluidFM 技术在跨学科研究中的关键支撑作用。

多功能单细胞显微操作系统- FluidFM OMNIUM
| 点击此处,即刻咨询前沿设备! |
西湖大学团队的最新研究成果以《Water-regulated viscosity-plasticity phase transitions in a peptide self-assembled muscle-like hydrogel》为题荣登Nature Communications期刊,为小分子自组装材料领域带来突破性进展。研究发现,四肽YAWF能自组装成类肌肉液晶水凝胶(LCH),在水调控下实现粘度-塑性相变,仅用2 μL凝胶就能拉制出超1 m长的固体纤维,还能承载自身250倍的重量。在这场材料科学的重大突破中,FluidFM 技术扮演了关键角色,为超精细纤维的力学性能分析提供了核心支撑。

“肌肉状水凝胶” YAWF
西湖大学团队研究发现,凭借YAWF特殊的氨基酸序列,在水中实现自组装,形成具有强各向异性的液晶水凝胶,其行为与人体肌肉高度相似:无外力时呈松弛状态,受力后纳米管定向排列,拉伸超过弹性范围时还会发生弹性-塑性转变。通过外力拉伸结合水调控结晶,这种超粘稠水凝胶能快速脱水固化,形成稳定的宏观纤维。
实验中,研究人员用移液枪手动拉伸就能得到长度超10 cm的超细纤维,规模化制备时长度更是突破1 m,且全程无需复杂修饰或添加剂,仅靠 pH 调节和水含量控制即可实现。这一发现不仅刷新了对小分子自组装潜力的认知,也为功能材料的低成本规模化制备提供了新路径。
FluidFM技术:超细纤维力学性能的精准标尺
要让这种新型材料走向应用,精准表征其力学性能是关键,而这正是 FluidFM 技术大显身手的地方。手工拉制的超细纤维直径仅数百纳米至10微米,传统力学测试方法难以精准捕捉其弹性模量,而 FluidFM 技术的介入有效解决了这一难题。
FluidFM技术的核心优势在于能对超精细、易损伤的样品进行无损力学探测。在本研究中,其作用主要体现在两方面:
精准适配超细样品:配备300纳米孔径的纳米移液管,能稳定捕捉直径仅数百纳米的YAWF纤维,避免测试过程中样品断裂或变形,解决了传统设备 “抓不住、测不了” 的困境。
定量分析弹性模量:通过方程拟合测试数据,成功测定12根超细纤维的杨氏模量,弥补了传统动态力学分析(DMA)对超细样品测量的局限性,为材料力学性能提供了精准数据支撑。
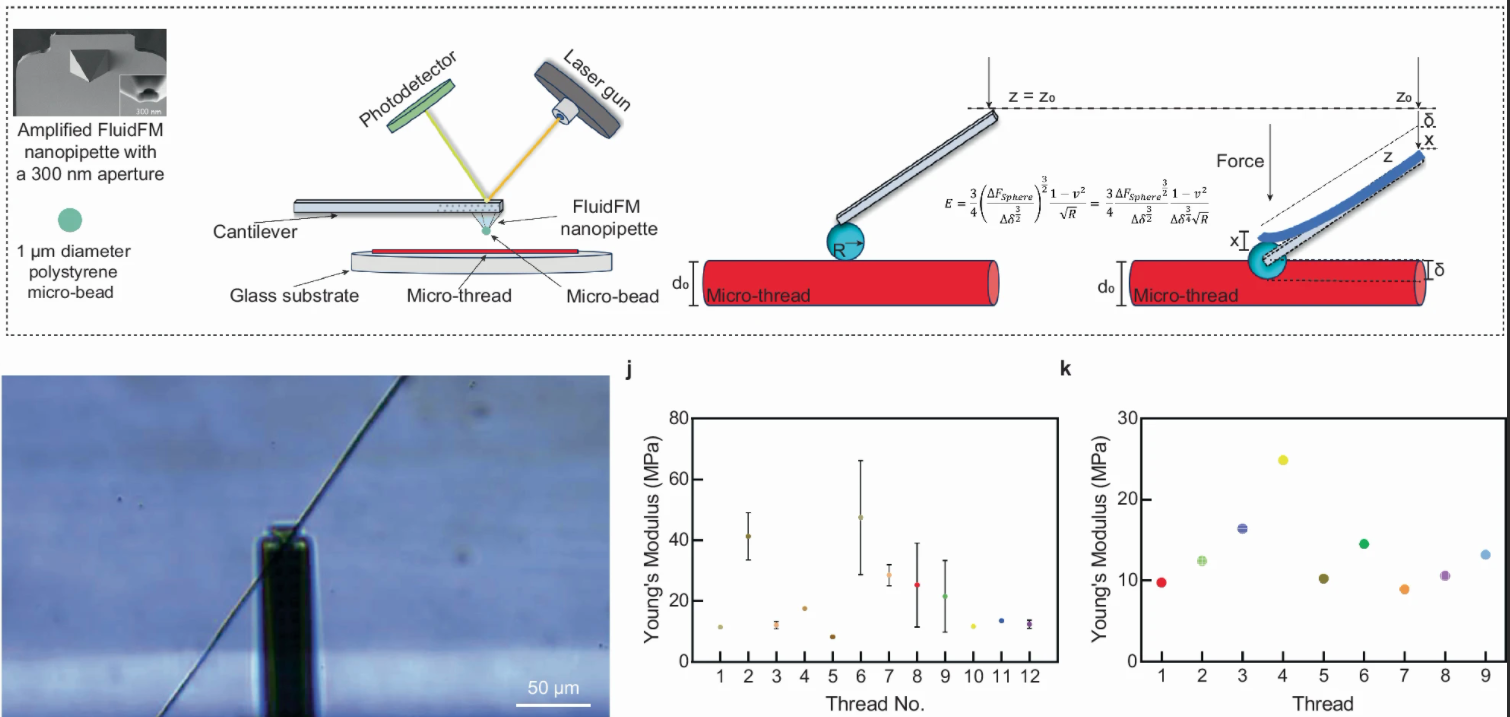
正是借助 FluidFM 技术的精准测量,西湖大学团队证实:YAWF 纤维的杨氏模量与拉伸速率正相关,且即使是超细纤维,其力学强度仍能满足实际应用需求,为后续材料优化提供了关键依据。这一技术突破让超细材料的力学表征从 “定性描述” 迈入 “定量分析” 的新阶段。
未来可期:从 Nature 突破到应用落地
这种兼具生物相容性、可回收性和超高力学性能的材料,未来应用场景十分广阔。在人工肌肉领域,其类肌肉的相变特性可用于研发更灵敏的柔性执行器;在 wearable 电子设备中,低成本、易成型的优势能降低器件制造门槛;在生物医学领域,生物可降解特性使其有望成为新型药物载体或组织工程支架。
而 FluidFM 技术的成功应用,不仅为本次西湖大学的研究提供了关键数据,更为各类超细功能材料的力学表征提供了范例。它打破了传统测试技术的尺寸限制,让 “看得见、测不准” 的超细材料性能变得清晰可量化,加速了新型纳米组装材料的研发进程。
今年内,继西湖大学凭借“肌肉状水凝胶”研究登上Nature Communications后,国内科研界陆续传来捷报。北京大学工学院黄建永课题组借助 FluidFM 技术,在细菌与宿主粘附调控机制研究中取得突破性进展,相关成果正式发表于Journal of Controlled Release。从材料科学到生物医学,FluidFM 技术正持续赋能国内团队,在国际期刊上不断刷新 “中国科研实力”。

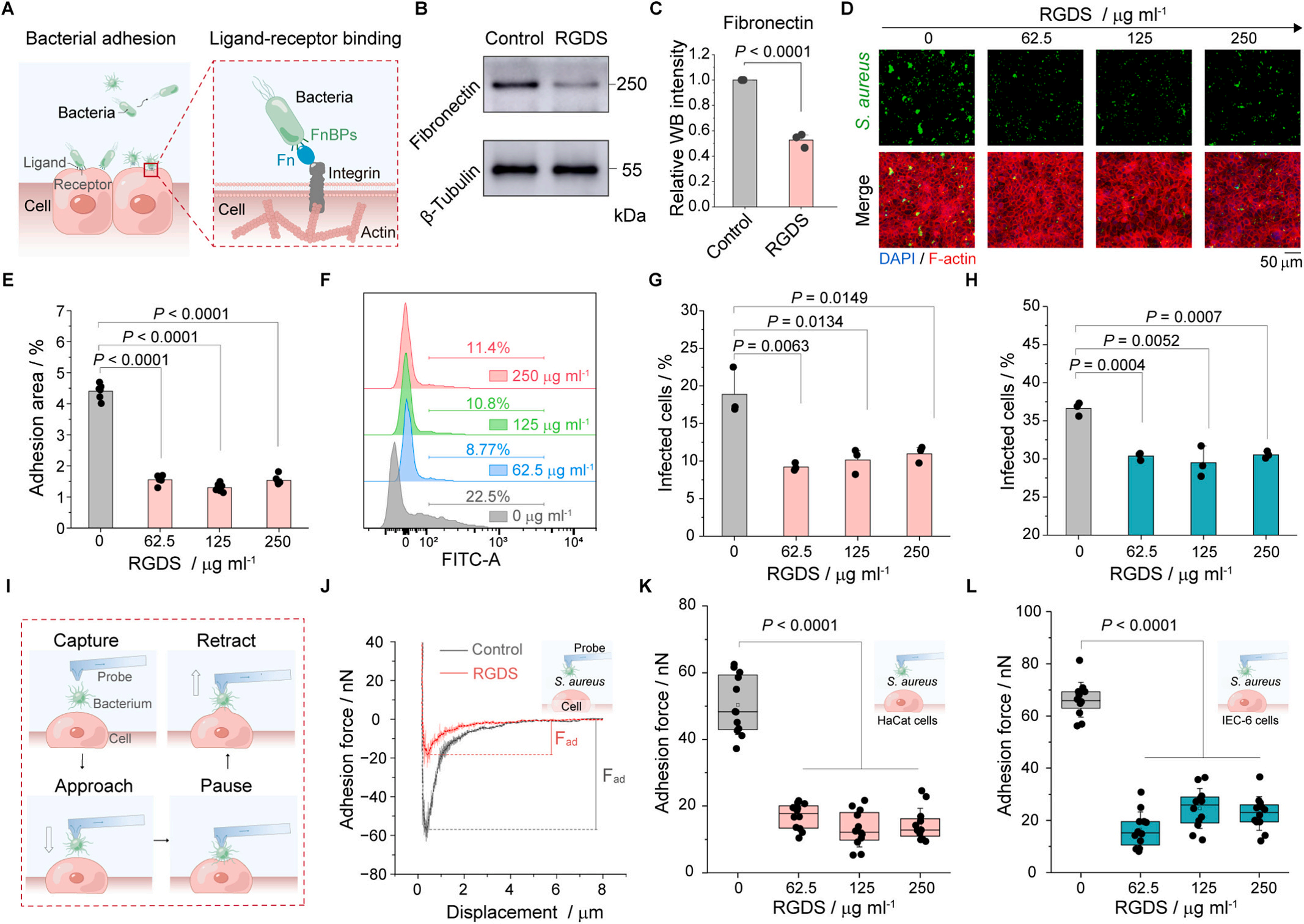
该研究中,FluidFM 的核心作用:
精准捕获:FluidFM探针可通过施加负压,像一只微型的“纳米吸管”一样,精准地捕获单个活体细菌(如金黄色葡萄球菌)。
可控接触:探针携带着单个细菌,精确控制地接近经过RGDS肽处理或未处理的宿主细胞(如人角质形成细胞HaCaT)。
实时测力:当细菌与细胞表面接触并短暂停留后,探针按设定程序回撤。在这个过程中,FluidFM实时、高精度地测量细菌与细胞表面分离所需的力——这就是细菌-宿主界面的黏附力(Adhesion Force)。
量化比较:通过对比处理组和对照组测得的黏附力数据,FluidFM提供了直接、定量、单细胞水平的证据。
FluidFM:国内科研的 “高水平期刊助力神器”
不止北大和西湖大学,FluidFM 技术已成为国内多领域科研团队的“得力助手”。浙江大学团队曾借助该技术研发天然粘合剂基纳米药物,精准测量纳米药物与细胞的粘附力,实时观察酸性肿瘤微环境中的药物作用过程,相关成果发表于 Biomaterials;北京大学2024年更凭借其“操作简单、适用细胞广、通量高、力学范围宽”的优势,一个月内斩获三篇单细胞力学领域重量级成果。
1. https://www.nature.com/articles/s41416-024-02861-x (published on October 11, 2024)
2. https://www.science.org/doi/10.1126/sciadv.adp0631 (published on November 1, 2024)
3. https://www.nature.com/articles/s41522-024-00600-x (published on November 12, 2024)
从材料科学的超精细纤维表征,到生物医学的细菌感染机制解析,再到肿瘤免疫疗法的纳米药物研发,FluidFM技术正在跨领域赋能国内科研创新。而西湖大学、北京大学等团队的持续突破,不仅展现了中国科研在基础研究领域的硬实力,更印证了“高端技术工具 + 原创科研思路”的高效模式,为中国科研走向国际前沿注入了强劲动力。
| 若您对设备有任何问题,欢迎扫码咨询! |
